삼천당제약, 아일리아 시밀러 연내 유럽 승인 전망…글로벌 진출 '속도'
컨텐츠 정보
- 7 조회
- 0 추천
- 목록
본문
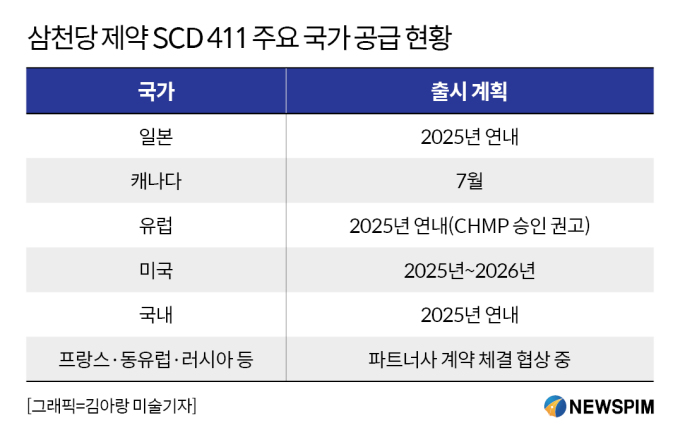
[서울=뉴스핌] 김신영 기자 = 삼천당제약의 안과질환 치료제 아일리아 바이오시밀러가 연내 유럽에서 품목 허가를 받을 가능성이 커졌다. 캐나다에 이어 유럽 출시가 가시화되면서 글로벌 시장 진출에 속도가 붙고 있다.
기존 바이알 제형 대비 치료 편의성이 높은 프리필드 시린지(PFS) 제형을 내세워 시장 공략에 나선 가운데 경쟁 우위를 점할 수 있을 지 주목된다.
 |
25일 업계에 따르면 삼천당제약은 아일리아 바이오시밀러 VGENFLI·EIYZEY(개발명 SCD411·성분명 애플리버셉트)에 대해 유럽의약품청(EMA) 산하 약물사용자문위원회(CHMP)로부터 판매 승인 권고를 받았다.
CHMP는 의약품의 안전성과 효과를 평가해 승인 권고를 결정하며, 권고 이후 빠르면 1~2개월 내에 유럽집행위원회(EC)로부터 최종 판매 승인을 얻게 된다. 유럽에서 오는 11월 오리지널 의약품인 아일리아의 특허가 만료되는 점을 고려할 때, 연내 판매가 시작될 가능성도 제기된다.
삼천당제약이 유럽 승인 권고를 받은 제품은 바이알 및 PFS 제형이다. 바이알의 경우 의료진이 주사기로 약물을 직접 뽑아서 투여해야 하는 반면, PFS는 약물이 미리 주사기에 충전돼 있는 제형으로 치료 편의성이 높다. 유럽에서 아일리아 시밀러를 PFS 제형으로 최초 승인 신청한 사례로, 시장 입지 확보에 유리하게 작용할 것이라는 관측이 나온다.
삼천당제약은 앞서 SCD411의 첫 수출 물량을 캐나다로 선적했다. 판매는 7월부터 본격적으로 개시될 예정이다. 선적된 물량 중 약 90%가 PFS 제형으로, 글로벌 시장에서 최초로 상용화될 전망이다. 회사는 이를 통해 글로벌 시장 선점에 한발 앞설 수 있을 것이라는 자신감을 내비치고 있다.
미국과 일본 진출 준비도 순항 중이다. 미국에서는 2023년 아일리아 특허가 만료돼 바이오시밀러의 시장 진입이 가능해진 상황이다. 삼천당제약은 지난해 12월 미국 파트너사 '프레제니우스 카비'와 독점 공급계약을 맺었다. 출시 시점은 이르면 연내 혹은 내년이 될 것으로 전망된다. 미국 시장 진출을 먼저 시도한 국내 바이오시밀러 기업들이 특허 소송에 부딪힌 가운데, 삼천당제약은 이에 대비해 PFS와 관련해 고유 제형 특허 등을 확보해 둔 상태다.
SCD411 미국 계약에는 고용량 제품도 포함됐다. 회사는 고용량 제형 특허 회피를 위한 제형을 개발한 상태로 조기 시장 진입을 자신하고 있다. 아일리아 시밀러 고용량 제형에 대한 특허는 2039년까지 보호되나, 삼천당제약은 특허 회피 제형을 기반으로 2028년 시장에 진입하겠다는 전략이다.
일본 파트너사와도 이미 계약을 맺고 허가 심사를 진행 중이다. 연내 출시 가능성에 무게가 실리고 있다. 다만 삼천당제약은 구체적인 일정은 공시 사항으로 언급하기 어렵다는 입장이다. 일본에서는 아직 국내 기업이 아일리아 시밀러 허가를 받은 사례는 없으며, 시장 진입을 준비 중인 단계다. 삼천당제약이 최초로 일본 시장에 진출할 지 주목된다.
삼천당제약은 미국과 캐나다, 일본 등 현재까지 공급 계약을 맺은 파트너사로부터 받게 될 계약금과 마일스톤 규모는 총 2400억원 이상이라고 밝힌 바 있다. 아일리아는 황반변성과 당뇨망막병증 등 안과질환의 대표적인 블록버스터 약물인 만큼 시장 진입을 계기로 매출 성장과 점유율 확대가 본격화될 것으로 기대된다.
삼천당제약 관계자는 "유럽에서 아일리아 바이오시밀러의 특허가 만료되는대로 자사 제품 판매를 시작할 계획"이라며 "SCD411의 주요 국가 진출에 따른 구체적인 매출 목표는 적절한 시기가 되면 공개하겠다"고 말했다.
관련자료
-
이전
-
다음

 월천해선 -
월천해선 - 
